वैलेंन्सी और वेलेंस इलेक्ट्रॉनों के बीच अंतर | वैलेंन्सी बनाम वेलेंस इलेक्ट्रानन
मुख्य अंतर - वैलेंसी बनाम वेलेंस इलैक्ट्रॉन
वैलेंसी इलेक्ट्रान और वेलेंस इलैक्ट्रॉन अंतर-संबंधित शब्द हैं, और महत्वपूर्ण अंतर औपचारिकता और ध्रुवीय इलेक्ट्रॉनों के बीच उनकी परिभाषा में सबसे अच्छा समझाया गया है; valence इलेक्ट्रॉनों एक तत्व के बाहरीतम खोल में इलेक्ट्रॉन हैं जबकि valency electrons इलेक्ट्रॉनों की संख्या है जिसे स्वीकार करने या निकाले जाने के लिए निकटतम महान गैस विन्यास । यह बाह्यतम खोल में इलेक्ट्रॉन है जो आम तौर पर रासायनिक बांड के रूप में योगदान करते हैं। कुछ परमाणुओं में, वैलिन्स इलेक्ट्रानों की संख्या वैलेंसी इलेक्ट्रॉनों की संख्या के बराबर होती है।
वी अलेंस इलेक्ट्रान क्या हैं? एक परमाणु के बाहरी छोर में इलेक्ट्रॉनों की संख्या को "वेलेंस इलैक्ट्रॉन" कहा जाता है इस कारण के कारण, एक परमाणु के बाह्यतम खोल को "वैलेंस शेल" कहा जाता है ज्यादातर समय, ये इलेक्ट्रॉन होते हैं, जो रासायनिक बंधन में भाग लेते हैं। जब तत्व सूत्र बनाते हैं, तो वे वैलेंस शेल से इलेक्ट्रॉनों को हटा देते हैं। एक तत्व में वैलेंस इलेक्ट्रॉनों की संख्या आवधिक तालिका में समूह निर्धारित करती है।
वैलेंन्सी इलेक्ट्रॉनों क्या हैं?

- तालिका से पहले अंतर आलेख मध्य ->
मुख्य समूह तत्वों की वैवाहिकता धातु तत्वों के लिए,
|
वालिन्स इलेक्ट्र्रॉन:
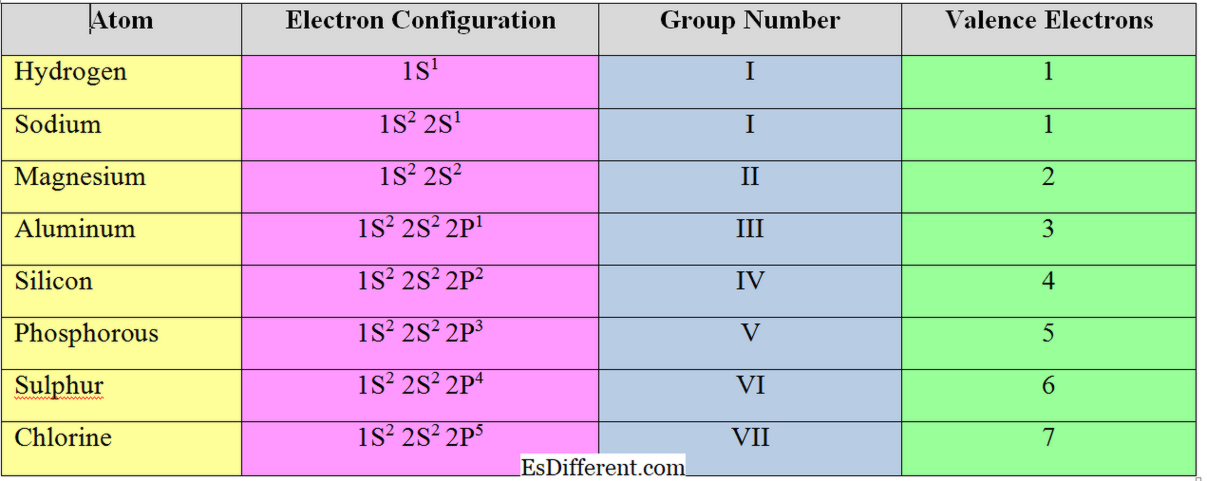
एक परमाणु के बाहरी छोर में इलेक्ट्रॉनों को "वेलेंस इलैक्ट्रॉन" कहा जाता है "एस" और "पी" समूह तत्वों के लिए, वेलेन्स इलेक्ट्रॉनों की संख्या उनके समूह संख्या के बराबर होती है।
उदाहरण वैलेंन्सी इलेक्ट्रॉन: निकटतम महान गैस के इलेक्ट्रॉन विन्यास को प्राप्त करने के लिए स्वीकार किए जाने या निकाले जाने वाले इलेक्ट्रॉनों की संख्या को "वीजेन्सी इलेक्ट्रॉन" या परमाणु के "वालिन्स" कहा जाता है।
सामान्य तौर पर, धातु के तत्वों (समूह I, II और III में तत्व) के लिए, वैलिन्स इलेक्ट्रानों की संख्या, योग्यता इलेक्ट्रॉनों की संख्या के बराबर होती है; ओक्टेट संरचना को प्राप्त करने के लिए वे वैलेंस शेल में इलेक्ट्रॉनों को हटा देते हैं।
लेकिन, गैर धातु तत्व निकटतम महान गैस के इलेक्ट्रॉन विन्यास को प्राप्त करने के लिए इलेक्ट्रॉनों को स्वीकार करते हैं। इसलिए, गैर-धातु तत्वों की औपचारिकता को कुल वीर्य इलेक्ट्रॉनों को 8 से घटाकर गणना की जाती है। क्लोरीन के लिए, वेंटेंसी इलेक्ट्रानों की संख्या = 8-7 = 1
वैलेंसी और वेलेंस इलेक्ट्रानिक्स के लक्षण
वैलेंसी और समूह VIII तत्वों के वाल्ले इलेक्ट्रॉनों
वेलेंस इलेक्ट्रानस:

समूह आठवीं तत्व, महान गैस हैं, और वे रासायनिक रूप से स्थिर हैं। उनका बाहरी कवच पूरा हो गया है, और इसमें बाहरी इलेक्ट्रॉनों (हीलियम -He को छोड़कर) में आठ इलेक्ट्रान शामिल हैं; ताकि समूह आठवीं इलेक्ट्रॉनों में आठ संयम इलेक्ट्रॉन होते हैं।
वैलेंन्सी इलेक्ट्रॉन:
वैलेंेंसी अन्य तत्वों या अणुओं के साथ बांड बनाने की क्षमता का एक उपाय है नोबल गैसों ने ओकटेट नियम को प्राप्त करने के लिए इलेक्ट्रॉनों को स्वीकार नहीं किया है या नहीं हटाया है क्योंकि वे पहले से ही अंतिम शेल पूरा कर चुके हैं। इसलिए, शून्य के बराबर समूह सातवीं तत्वों का मूल्य निर्धारण छवि सौजन्य:
"इलेक्ट्रॉन शेल 010 नियॉन - कोई लेबल नहीं" कॉमन्स द्वारा: उपयोगकर्ता: पम्मा (सामान्य कामकाज: उपयोगकर्ता: ग्रेग रॉबसन) - // commons। विकिमीडिया। संगठन / विकी / श्रेणी: इलेक्ट्रॉन_शेल्_आइट्रैग (संबंधित लेबल संस्करण)। (सीसी बाय-एसए 2. 0 यूके) कॉमन्स के माध्यम से


