एसिड-बेस टाइटेनेशन और रेडॉक्स टाइटटेशन के बीच का अंतर
मुख्य अंतर - एसिड-बेस टाइटलेशन बनाम रेडॉक्स टिट्रेशन
सामान्य तौर पर, एक अज्ञात समाधान (विश्लेषक) की एकाग्रता का निर्धारण करने के लिए इसका उपयोग किया जाता है। सबसे अधिक इस्तेमाल किया जाने वाला दो titrimetric तरीकों एसिड-आधार titrations और redox titrations हैं। प्रमुख अंतर एसिड-बेस टाइटेनेशन और रेडॉक्स टिटेशंस के बीच टिपट्रिंट और विश्लेषक के बीच होने वाली प्रतिक्रिया की प्रकृति है अनुमापन में एसिड-बेस्ड टाइट्रेशन में, एक निष्पक्ष प्रतिक्रिया होती है और रेडॉक्स टिटेशन्स में, एक रेडॉक्स प्रतिक्रिया होती है (एक ऑक्सीकरण प्रतिक्रिया और कमी प्रतिक्रिया)। संकेतक का उपयोग प्रतिक्रिया की समाप्ति बिंदु निर्धारित करने का सबसे अधिक इस्तेमाल किया जाने वाला तरीका है।
एसिड-बेस टाइटेशन क्या है?
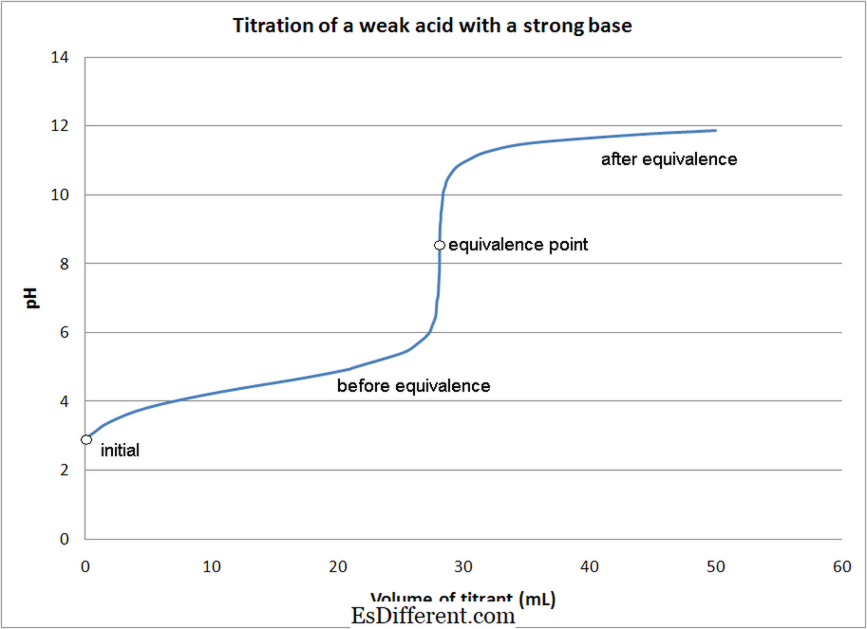
एसिड-बेस्ड टाइट्रेशन में, एसिड (अम्लीय टिटस्ट्रेशन) या बेस (बेसिक टाइटस्ट्रेशन) का उपयोग टिपेंटर के रूप में किया जाता है अम्लीय अनुक्रमों में प्रयुक्त एसिड के उदाहरण एच 2 SO 4 , एचसीएल, या एचएनओ 3 ज्यादातर मूलभूत उपयोगिताएं नाओएच, के 2 सीओ 3 या ना 2 सीओ 3 एसिड-आधार का नामकरण एसिड की ताकत और बेस के आधार पर निम्नानुसार वर्गीकृत किया जा सकता है सशक्त एसिड - मजबूत आधार लेखांकन सशक्त एसिड-कमजोर आधार अनुरेखण
कमजोर एसिड - मजबूत आधार उपशमन- कमजोर एसिड - कमजोर आधार उपन्यास
- अधिकांश एसिड में -बेज टिटस्ट्रेशन, संकेतक प्रतिक्रिया का अंत बिंदु निर्धारित करने के लिए उपयोग किया जाता है। विभिन्न संकेतकों का प्रयोग ऊपर वर्णित टिटेशंस के प्रकार के आधार पर किया जाता है।
- एक रेडॉक्स टाइटलेशन क्या है?
एक रेडॉक्स निदान में एक रेडॉक्स प्रतिक्रिया शामिल है रेडॉक्स प्रतिक्रिया में दो प्रतिक्रियाएं हैं; एक ऑक्सीकरण प्रतिक्रिया और कमी प्रतिक्रिया। दोनों ऑक्सीकरण और कमी की प्रक्रिया एक ही समय में होती है जहां हमें प्रतिक्रिया को पूरा करने की इजाजत दी जाती है। यह अनुमापन के अंत बिंदु के रूप में भी जाना जाता है। यह कई मायनों में निर्धारित किया जा सकता है; सूचक इलेक्ट्रोड, रेडॉक्स संकेतक (सूचक ऑक्सीकरण कमी राज्य पर एक अलग रंग का उत्पादन), और गैर-रेडॉक्स संकेतक का उपयोग करते हुए (संकेतक एक रंग का उत्पादन करते हैं, जब एक अधिक मात्रा में पेटेंट जोड़ा जाता है)।
प्रतिक्रिया की प्रकृति:
एसिड-बेस टाइटेशन:

एसिड-बेस टिटस्ट्रेशन में विश्लेषक (अज्ञात एकाग्रता के साथ समाधान) और अम्लीय या मूल लेखिका के बीच एक निष्पक्ष प्रतिक्रिया शामिल है।
रेडॉक्स टाइटेशन:
एक रेडॉक्स प्रतिक्रिया में विश्लेषक और पेटेंट के बीच ऑक्सीकरण और कमी की प्रतिक्रिया शामिल है। ऐसा कोई ऐसा नियम नहीं है कि घटक ऑक्सीडीज होता है और जो कम हो जाता है या तो विश्लेषक या तीक्ष्ण ऑक्सीडीज, और शेष घटक तदनुसार कम कर देता है। समापन बिंदु का निर्धारण: एसिड-बेस टाइटेशन:
सामान्य तौर पर, पीएच संकेतक, पीएच मीटर या एक प्रवाहकत्त्व मीटर का उपयोग एसिड-बेस टिटस्ट्रेशन के अंत बिंदु को निर्धारित करने के लिए किया जाता है। रेडॉक्स टाइटेशन: रेडॉक्स प्रतिक्रिया के अंत बिंदु को निर्धारित करने के सबसे अधिक इस्तेमाल किए जाने वाले तरीके एक पोटेंशियोमीटर या रेडॉक्स सूचक का उपयोग कर रहे हैं। लेकिन, अक्सर या तो विश्लेषक या लेखिका अंत बिंदु पर रंग का उत्पादन करते हैं। इसलिए, उन मामलों में अतिरिक्त संकेतक की आवश्यकता नहीं है।
उदाहरण:
एसिड-बेस टाइटेशन: - अंतर लेख तालिका ->
प्रकार प्रतिक्रिया (संकेतक)
सशक्त एसिड - मजबूत आधार निदान
एचसीएल + नाओहाएनएएल + एच
2| हे (फेनोल्फिथेलिन / मिथाइल नारंगी) | मजबूत एसिड - कमजोर आधार निदान |
| एचसीएल + एनएच | 3 एनएएच 3 |
| सीएल (मिथाइल नारंगी) | कमजोर एसिड - मजबूत आधार अनुमापन सीएच 3 सीओओएचएचएच + नाओएचएएचएच सीएच 3 COONA + एच |
| 2 | ओ (फेनोल्फिथेलिन) कमजोर एसिड-बेस बेस अनुमापन सीएच 3 COOH + NH 3 एएच |
| 3 | सीओओ - एनएच 4 + (कोई उपयुक्त संकेतक नहीं) रेडॉक्स टिटेटेशन: 2 केएमएनओ 4 + 5 एच 2 सी 2 |
ओ 4
+ 6 एचसीएल → 2 एमएनसीएल 2 + 2KCl + 10 CO 2 +8 एच 2 ओ (+7) (+3) (+2) (+ 4) उपरोक्त प्रतिक्रिया में, ऑक्सीलिक एसिड ऑक्सीकरण किया जाता है, जब परमैनेटेट कम हो जाता है। जब प्रतिक्रिया पूरी होती है, परमैंगनेट के बैंगनी रंग में रंगहीन होता है। केएमएमओ 4 + 5 एफईसीएल 2 +8 एचसीएल → 5 एफईसीएल
3
+ एमएनसीएल 2 + केएल + 4 एच
2 ओ (+7) (+2) (+3) (+2) चित्र सौजन्य: 1 क्वांटमकिनेटिक्स (स्वयं के काम) [सीसी बाय 3. 0], विकिमीडिया कॉमन्स 2 के माध्यम से मजबूत आधार वाले कमजोर एसिड का ट्यूटेटेशन विलवर्ड द्वारा "विंकलर टाइटटेशन प्री टिटेटेशन" [सीसी बाय-एसए 3. 0] कॉमन्स के माध्यम से



