फेरस ग्लुकोनेट और फेरस सल्फेट के बीच अंतर
फेरस ग्लूकोनेट बनाम फेरस सल्फेट
आयरन एक प्रतीक है जिसमें प्रतीक एफई के साथ डी ब्लॉक में एक धातु है। यह धरती बनाने वाले सबसे आम तत्वों में से एक है और पृथ्वी के भीतर और बाहरी केंद्र में बड़ी मात्रा में है। पृथ्वी की पपड़ी में यह चौथा सबसे आम तत्व है लोहे में 2 से +8 तक के ऑक्सीडेशन राज्य हैं इनमें से +2 और +3 रूप सबसे आम हैं। +2 लोहे के ऑक्सीकरण फार्म को लौह और +3 रूप को फेरिक कहा जाता है। ये आयन ईओण क्रिस्टल के रूप में होते हैं, जो विभिन्न आयनों के साथ बनते हैं। विभिन्न प्रयोजनों के लिए जैविक प्रणालियों के लिए लोहे की आवश्यकता है उदाहरण के लिए, मानव में, लौह हीमोग्लोबिन में चीलेटिंग एजेंट के रूप में पाया जाता है। पौधों में क्लोरोफिल संश्लेषण के लिए यह भी महत्वपूर्ण है इसलिए, जब इस आयन की कमी होती है, जैविक प्रणाली विभिन्न रोगों को दिखाती है। लौह ग्लूकोनेट और फेरस सल्फेट दो आयनिक यौगिक हैं जो कि रहने वाले प्रणालियों में लौह की कमियों को दूर करने के लिए लौह खुराक के रूप में दिए जा सकते हैं।
लौह ग्लूकोनेट
ग्लूकॉनिक एसिड के लोहे के लवण में से एक को लौह ग्लूकोनेट कहा जाता है ग्लासोकैनीक एसिड का कार्बोक्जिलिक एसिड समूह इस नमक का उत्पादन करने के लिए लौह के साथ प्रतिक्रिया करता है। इस नमक का उत्पादन करते समय दो ग्लूकोनेट आयन लोहे के आयन के साथ बातचीत कर रहे हैं। इसमें सी 12 एच 24 FeO 14 का आणविक सूत्र है। यौगिक के दाढ़ जन 448 है। 15. लौह ग्लूकोनेट में निम्नलिखित संरचना होती है।
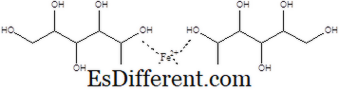
फर्गोन, फेरैलैट, और सिमरन जैसे ब्रांड नामों के तहत विपणन किया जाता है। हाइपोहोर्मिक एनीमिया जैसे रोगों के लिए, जो शरीर में लोहे की कमी के कारण होता है, लौह ग्लूकोनेट को दिया जाता है। इसके अलावा, फेरस ग्लूकोनेट को एक खाद्य योज्य के रूप में प्रयोग किया जाता है। -3 -> फेरस सल्फेट
लौह सल्फेट रासायनिक सूत्र FISO4
के साथ एक आयनिक यौगिक है। यह पानी के अणुओं की मात्रा के आधार पर अलग-अलग क्रिस्टल प्रकारों में मौजूद हो सकता है। इसमें निर्जल पदार्थ, मोनोहाइड्रेट, टेट्राहाइड्रेट, पेंटायहाइड्रेट, हेक्साहाइड्रेट और हेप्टाहाइड्रेट रूप हैं। इनमें से, नीले, हरे रंग के हेप्टाहाइड्रेट का रूप आम है Monohydrate, pentahydrate और hexahydrate रूप अपेक्षाकृत दुर्लभ हैं। नीले, हरे रंग के क्रिस्टल के अलावा, फेरस सल्फेट के अन्य रूप ज्यादातर सफेद रंग का क्रिस्टल हैं। जब हाइड्रेटेड क्रिस्टल को ढीले पानी गरम किया जाता है और निर्जल ठोस बन जाता है और हीटिंग के बाद, यह सल्फर डाइऑक्साइड, सल्फर ट्रायऑक्साइड और लोहा (III) ऑक्साइड (लाल भूरे रंग का रंग) में विघटित हो गया है।वे बिना गंध क्रिस्टल हैं फेरस सल्फेट आसानी से पानी में घुलता है और उस मामले में, फेरस आयन हेक्सा एक्वा कॉम्प्लेक्स बनाता है [Fe (H 2 O) 6 ] 2+ लोहे की कमी वाले एनीमिया जैसे लोहे की कमी की स्थिति का इलाज करने के लिए फेरस सल्फेट का उपयोग किया जाता है। न केवल मानवों के लिए, यह पौधों में भी जोड़ा जाता है, साथ ही साथ। लोहे क्लोरोसिस जैसी स्थितियों में, जहां पौधे पत्ते पीले हो जाते हैं, पीले रंग के लौह को दिया जाता है। इसके अलावा, यह अन्य यौगिकों को संश्लेषित करने के लिए अग्रदूत के रूप में उपयोग किया जाता है। चूंकि यह एक कमी एजेंट है, इसका इस्तेमाल रेडॉॉक्स प्रतिक्रियाओं के लिए भी किया जाता है। फेरस ग्लूकोनेट और फेरस सल्फेट के बीच अंतर क्या है?



